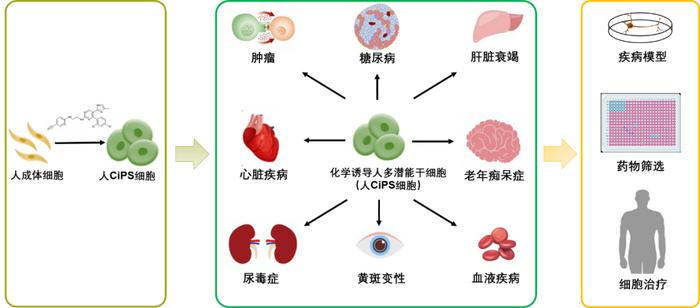
北京大学邓宏魁教授团队在国际顶级学术期刊《自然》(Nature)上发布了我国自主研发的新一代人多潜能干细胞制备技术,标志着我国在干细胞与再生医学这一前沿科技领域的原始创新能力取得了重大突破。该技术不仅为未来细胞治疗、疾病模型构建及药物筛选等应用提供了更为安全、高效的“种子细胞”来源,也为我国在生物医药领域的自主可控发展注入了强劲动力。
多潜能干细胞(如胚胎干细胞和诱导多能干细胞)具有分化成人体内几乎所有细胞类型的潜力,是再生医学、发育生物学研究和药物发现的基石。长期以来,国际主流技术路线在诱导效率、安全性及制备成本等方面仍存在挑战。邓宏魁团队此次开发的新技术,通过创新的化学小分子组合与调控策略,成功实现了从人体体细胞(如皮肤细胞)向高质量多潜能干细胞的直接高效重编程。与以往依赖病毒载体导入外源基因的方法相比,该技术避免了基因组整合风险,且诱导过程更可控、均一性更高,所获得的干细胞在分化潜能和基因组稳定性上表现出优异特性,因而被视为“新一代”技术。
这一成果的取得,是我国科研人员长期坚持基础研究与前沿技术攻关的结晶。它体现了从“0到1”的原始创新,其核心在于团队对细胞命运转换调控网络的深刻理解,并成功设计出能够精确模拟和操控这一网络的非整合式化学诱导方案。这为干细胞制备提供了一条全新的、具有自主知识产权的技术路径,有望降低相关技术对国外专利的依赖。
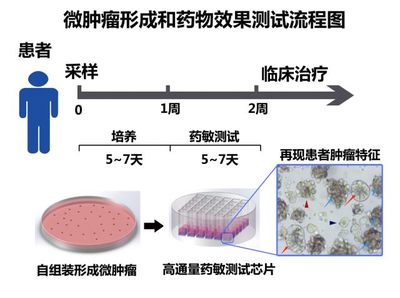
在应用前景方面,新一代技术将极大推动干细胞技术的研发和临床转化进程。在细胞治疗领域,该技术有望生产出更安全、合规的干细胞来源,用于治疗帕金森病、糖尿病、心肌梗死等重大疾病。在疾病模型方面,可以更容易地从患者体细胞获得多潜能干细胞,进而分化为病变器官的细胞(如神经元、肝细胞等),构建“患者特异性”疾病模型,用于病理机制研究和个性化药物筛选。该技术平台还可用于研究人类早期胚胎发育、细胞衰老等基础科学问题。
从实验室技术到成熟的产业化应用,仍需经历严格的工艺优化、安全性评估和临床试验验证。邓宏魁团队的研究无疑为后续的转化研究奠定了坚实的技术基础。这一突破也预示着,我国在生命科学和生物技术战略领域的布局正逐步结出硕果,通过持续加强基础研究和关键核心技术攻关,中国正稳步迈向全球细胞科技创新的前沿,为人类健康事业贡献中国智慧与中国方案。