3D生物打印技术作为再生医学和生物制造领域的尖端科技,正以前所未有的速度改变着人类对疾病治疗与组织修复的认知。清华大学机械工程系孙伟教授团队在这一领域的前沿探索,尤为引人注目。他们致力于将细胞技术、生物材料与精密制造相结合,让“打印”出具有活性与功能的人体器官,从科幻构想逐步走向现实应用。
一、 3D生物打印:从“形似”到“神似”的技术飞跃
传统的3D打印主要处理塑料、金属等无生命材料,而3D生物打印的核心在于“生物墨水”。这种墨水通常由活细胞、生物相容性材料和必要的生长因子混合而成。孙伟团队的研究重点之一,便是研发性能优异的生物墨水。他们不仅追求打印出的结构在形状上高度模拟真实器官,更致力于确保打印后细胞的存活、增殖、分化以及最终形成具有正常生理功能的组织。这要求生物墨水必须具备良好的打印成型性、细胞亲和性,并能提供适合细胞生长的微环境。
二、 核心技术:细胞技术的深度融入
细胞的获取、培养和定向诱导分化是3D生物打印成功的关键。目前,常用的细胞来源包括患者自身的干细胞(如间充质干细胞)、诱导多能干细胞(iPSC)或已分化的功能细胞。孙伟团队的工作深入到了细胞层面,探索如何在打印过程中及打印后,通过精确控制生物、化学及物理信号,引导细胞按照预定的三维结构进行有序排列和功能构建。例如,在构建骨组织时,需要引导干细胞向成骨细胞分化;在构建血管网络时,则需要内皮细胞和平滑肌细胞的协同作用。这一过程,本质上是将发育生物学和细胞生物学的原理,通过工程学的手段进行“编程”和“再现”。
三、 应用前景:从组织修复到器官再造的广阔蓝图
尽管打印出完整、复杂且可直接移植的实体器官(如心脏、肝脏)仍需攻克血管化、神经支配、免疫排斥等巨大挑战,但3D生物打印技术已在多个层面展现出巨大的应用潜力:
- 个性化组织修复:利用患者自身的细胞,打印出与缺损部位完美匹配的骨、软骨、皮肤等组织移植物,可极大降低免疫排斥风险,用于创伤修复或肿瘤切除后的重建。
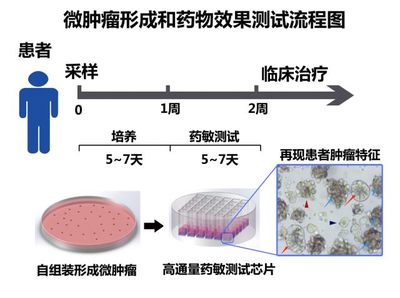
- 高仿生疾病模型:打印出包含多种细胞、具有特定三维结构的微型器官(如肝小叶、肿瘤模型),用于药物筛选和毒性测试。这种模型比传统的二维细胞培养和动物实验更能准确模拟人体内的真实反应,有望加速新药研发进程。
- 药物递送载体:将载有药物的生物材料与细胞一同打印,构建出能够靶向释放药物、同时促进组织再生的智能支架。
- 探索生命科学奥秘:通过构建可控的、简化的人体组织模型,为研究胚胎发育、疾病发生机制等基础科学问题提供了前所未有的工具。
四、 挑战与未来:通往临床的漫长征途
孙伟教授指出,当前3D生物打印技术走向大规模临床应用,仍面临一系列核心挑战:
- 生物墨水的多功能性与安全性:需要开发更多能模拟天然细胞外基质复杂功能的智能材料。
- 血管网络构建:如何快速、有效地在打印组织中构建起能够输送养分和氧气的毛细血管网络,是打印大体积、高代谢活性组织的瓶颈。
- 制造精度与速度的平衡:高精度打印往往耗时过长,影响细胞活性;提高速度又可能牺牲结构精度。需要开发新型打印工艺。
- 标准化与监管:作为涉及生命的医疗产品,其生产流程、质量控制、安全性和有效性的评价体系亟待建立和完善。
清华孙伟团队在3D生物打印领域的探索,代表了我国在该交叉学科前沿的坚实步伐。从精密的生物墨水配方,到细胞命运的精准调控,再到复杂器官结构的逐层构建,每一步都凝聚着工程学、材料学与生命科学的智慧结晶。尽管“打印”一个完全功能化的人体器官尚需时日,但这项技术正在并已经为个性化医疗、新药研发和基础生命科学研究开辟了革命性的路径。随着关键技术的不断突破,3D生物打印有望真正实现按需“制造”人体组织与器官的梦想,为人类健康带来深远影响。